Il y’a maintenant plusieurs années je m’étais intéressé à la réplication de l’ADN (Acide Désoxyribonucléique) et à son fonctionnement, je voulais vous synthétiser dans un petit article comment fonctionne cette double hélice essentielle au plus profond des cellules de notre corps.
Dans les bras de nos chromosomes, les télomères se trouvent nos gènes dans lesquels se trouve une structure à double hélice, j’ai nommé l’acide désoxyribonucléique.
Cherchons dans un premier temps un peu à analyser la structure orthographique de ce mot : désoxy peut faire penser à l’atome d’oxygène en moins, ribo peut faire penser au ribosome mais surtout à la ribose ou encore ribose et nucl veut surement signifier que les nucléotides se trouvent dans le noyau de la cellule.
Cet acide est composé de quatre bases : l’adénine, la guanine, la thymine et la cytosine.
Etudiez les bases nucléiques, c’est fondamental pour comprendre l’ADN, il existe deux types de bases, les bases puriques et les bases pyrimidiques, la grande différence entre les bases est le nombre de liaisons covalentes internes : une base pyrimidique forme 1 à 6 liaisons atomiques covalentes internes, une base purique en forme 1 à 9.
Alors comment ça marche ?

L’Acide a la forme d’une double hélice.
Voici le schéma que j’ai amélioré pour vous aider à comprendre, une petite explication s’impose. 5 et 3 sont les deux chiffres magiques qui vont déterminer le sens de lecture et le sens de synthèse dit réplication.
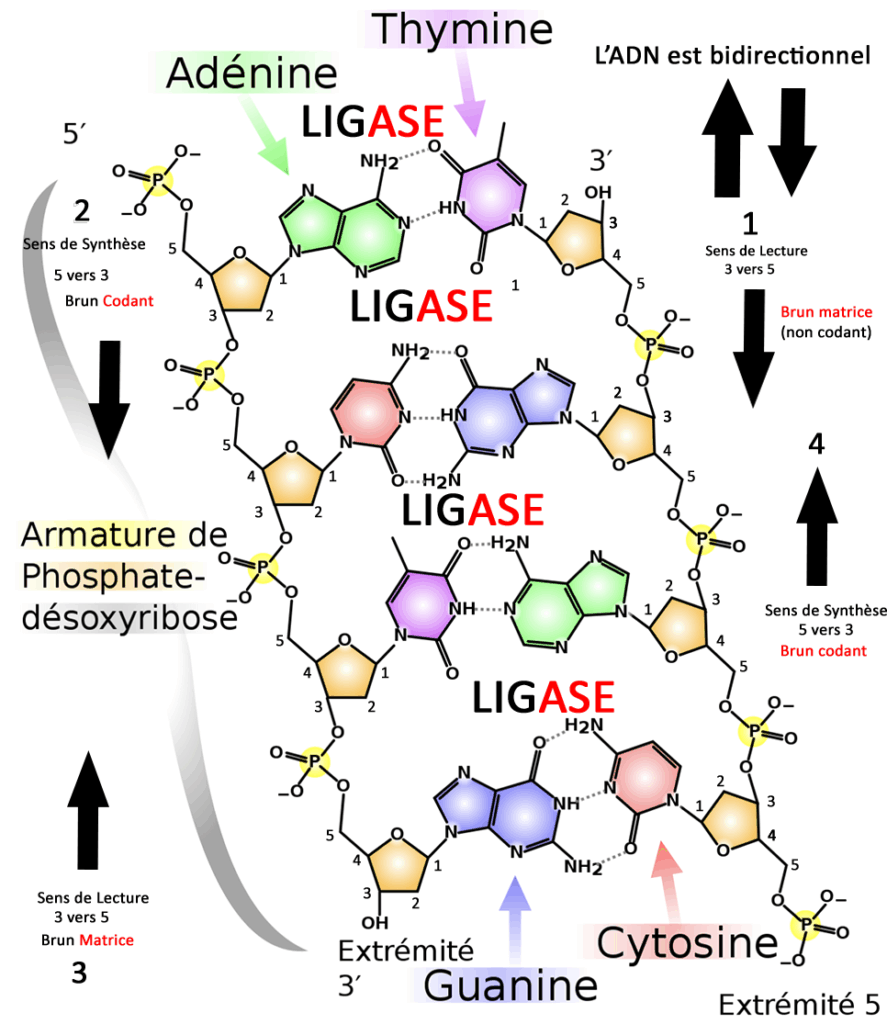
L’ADN est bidirectionnel de par sa forme en double hélice : la phase 1 est la lecture du brin matrice, en quelque sorte c’est le brin qui va servir de base pour la réplication, on le lit dans le sens 3 -> 5. Puis vient de l’autre côté la phase 2 de réplication dite de synthèse dans le sens des extrémités 5 -> 3. Le brin qui a été répliqué à gauche pendant la phase 2 va servir à son tour de brin matrice pendant la phase 3 dans le sens 3 -> 5. Pour finir le brin droit va continuer sa réplication dans le sens 5 -> 3.
La synthèse du brin de réplication(brin synthétisé ou néoformé) se base sur la lecture du brin inverse (brin matrice ou brin parental) dans le sens des extrémités 3 à 5, du 3ème atome de carbone qui forme le sucre ribose jusqu’au 5ème jusqu’à la liaison avec le phosphate.
Petit aparté, le phosphate est un ion phosphore oxydé par 4 atome d’oxygène et tous les composés qui se terminent par ate subissent l’effet de l’oxydation.
J’ai fait un graphique en deux dimensions ce qui n’est pas tout à fait convenable pour expliquer la structure en double hélice mais cela va vous aider à comprendre le principe. J’ai numéroté tous les atomes de carbone pour vous aider à comprendre le sens de réplication.
On veut synthétiser le brin gauche qui commence par la base Adénine (en vert) on sait que l’extrémité est 5, de l’autre côté le brin inverse de par la structure en double hélice, l’extrémité est 3 en haut donc le brin gauche va commencer par lire l’information (phase 1) puis la synthèse commence (phase 2).
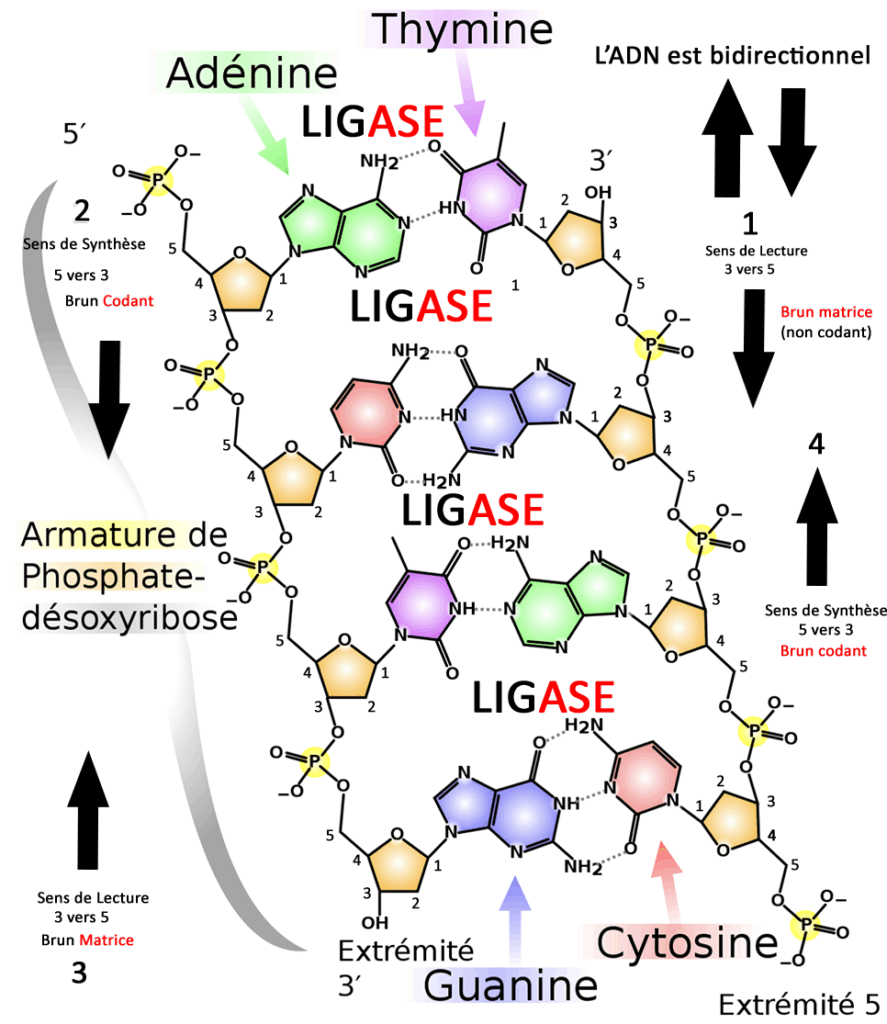
(phase 3) Par la suite on lit le brin gauche qui a été synthétisé en partant du bas dans le sens 3 à 5 à nouveau
( brin matrice) pour synthétiser le brin droit dans le sens 5 vers 3 (phase4)
L’ADN Ligase (lien catalyseur) est une enzyme qui va permettre aux bases respectives de se lier et de former l’acide.
Mais comment ca peut marcher aussi bien, il faut bien un début et une fin pour lire l’information et synthétiser ? Et bien vous avez raison L’ADN Primase qui est une ADN Polymérase l’enzyme qui amorce la réplication va avoir besoin des fragments d’Okazaki.
En effet lors de la réplication compte tenu de ce que nous avons déjà expliqué, nous ne pouvons répliquer les brins simultanément donc nous allons avoir un brin précoce qui sera répliqué et un brin tardif qui sera répliqué de manière discontinue grâce aux fragments brin bleu du bas.
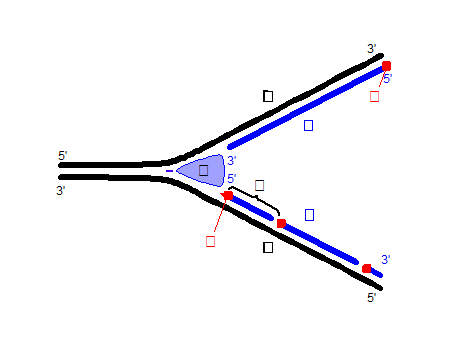
Fragments D’Okazaki



